HISTORIA CHEMII ANALITYCZNEJ W UNIWERSYTECIE ŁÓDZKIM
Badania naukowe z zakresu chemii analitycznej na Wydziale Matematyczno-Przyrodniczym UŁ rozpoczął inż. Bolesław Modrzejewski, który jako zastępca profesora kierował Zakładem Chemii Nieorganicznej od 1945 r. do września 1949r. Bolesław Modrzejewski intensywnie pracował nad tematem dotyczącym fotokolorymetrycznych oznaczeń związków siarki. Niestety oznaczanie siarczków metodą błękitu metylenowego zostało opublikowane przez innych naukowców. Bolesław Modrzejewski znany jest jako autor dwóch wydań wartościowej monografii naukowej „Pomiary pH”(WNT Warszawa 1952 r. wyd. 1 i 1971 r. wyd. 2).
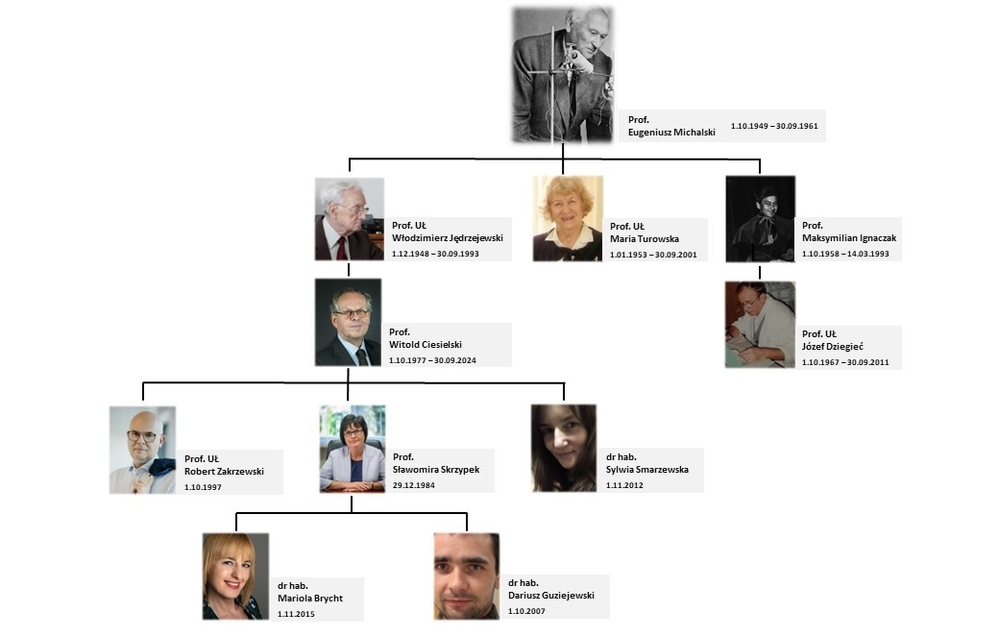
Intensywny rozwój chemii analitycznej nastąpił w czasie kierowania Zakładem Chemii Nieorganicznej od października 1949r. do września 1961r. przez prof. Eugeniusza Michalskiego. Profesor rozwijał metody amperometrycznego miareczkowania z wykorzystaniem stałych mikroelektrod wskaźnikowych zapoczątkowane przez niego na Uniwersytecie Stefana Batorego w Wilnie. Pod kierownictwem prof. Michalskiego rozpoczęto również prace z analizy kulometrycznej oraz analizy kinetycznej z wykorzystaniem amperometrycznej rejestracji przebiegu reakcji. Opracowano metody kinetycznych oznaczeń rodanków, siarczków i tiosiarczanów z wykorzystaniem indukowanej reakcji jodo-azydkowejoraz kinetycznych oznaczeń śladów jonów metali i jonów jodkowych. Lata pracy prof. Eugeniusza Michalskiego zaowocowały szeregiem doktoratów z chemii analitycznej uzyskanych przez pracowników Zakładu.
Uczniowie profesora Michalskiego: Włodzimierz Jędrzejewski, Maria Turowska i Maksymilian Ignaczak kontynuowali badania naukowe z zakresu chemii analitycznej.
Prof. Maria Turowska prowadziła badania nad wykorzystaniem chemiluminescencji pochodnych akrydyny do celów analitycznych. Opracowała nowe metody oznaczeń alkacymetrycznych z zastosowaniem pochodnych akrydyny jako wskaźników. Zaproponowała również metodę identyfikacji i oznaczania alkoholi. W latach 1963-93 prowadziła wykład z chemii analitycznej i kierowała laboratorium chemii analitycznej, wydała trzy skrypty studenckie.
Prof. Maksymilian Ignaczak ( kierował Katedrą Chemii Ogólnej i Nieorganicznej w latach 1978-1993) opracował metody miareczkowania szeregu związków organicznych roztworem chloranu(VII) ceru(IV). Postępowanie analityczne poprzedzone było badaniem zarówno kinetyki reakcji utleniania tych związków jak i mechanizmów zachodzących procesów utleniania. Pracę habilitacyjną pt. "Badania nad procesami utleniania alifatycznych kwasów karboksylowych za pomocą nadchloranu cerowego" przedstawił w 1971r. Podobną tematykę kontynuował prof. Józef Dziegieć, który obronił rozprawę habilitacyjną pt. "Kinetyka i mechanizmy reakcji ceru(IV) z niektórymi grupami związków organicznych oraz próby wykorzystania wyników tych badań w analizie ipreparatyce organicznej"
Prof. Włodzimierz Jędrzejewski, rozwinął kinetyczne metody analizy oraz metody kulometryczne. Pracę habilitacyjną pt. „Katalityczne reakcje utleniania niektórych połączeń siarki w analizie chemicznej” obronił w 1974r. Prof. Jędrzejewski w 1957r. zorganizował pierwszą w UŁ pracownię analizy instrumentalnej, następnie w miarę rozwoju metod instrumentalnych stale ją unowocześniał prowadząc jednocześnie wykłady z analizy instrumentalnej. Był współautorem dwóch skryptów studenckich zawierających ćwiczenia laboratoryjne z analizy instrumentalnej. Dzięki jego staraniom w 1978 r. został utworzony Zakład Analizy Instrumentalnej. W tym niewielkim zakładzie początkowo wypracowane zostały dwa kierunki badań: ligandy elektrochemicznie czynne w analizie jonów metali oraz reakcje indukowane w kulometrii.
W ramach pierwszego kierunku opracowano polarograficzne metody oznaczeń metali oparte na elektrochemicznej redukcji ligandów związanych w kompleks.
Prace związane tematycznie z drugim kierunkiem realizowane były w ramach problemu międzyresortowego MR. I. 32 i programu CPBP 01.17, koordynowanych przez prof. Adama Hulanickiego. W. Jędrzejewski i W. Ciesielski zaproponowali wykorzystanie miareczkowania kulometrycznego anodowo wytwarzanym jodem do oznaczania nieorganicznych i organicznych związków dwuujemnej siarki indukujących reakcję jodo-azydkową a także jonów metali tworzących kompleksy ze związkami siarki. W. Ciesielski przedstawił również spektrofotometryczne oznaczania induktorów reakcji jodo-azydkowej.
W 1991r. Witold Ciesielski obronił rozprawę habilitacyjną pt. „Reakcja jodo-azydkowa w aspekcie kulometrycznych i spektrofotometrycznych metod analizy”.
Po objęciu kierownictwa Zakładu Analizy Instrumentalnej w 1993r. przez Witolda Ciesielskiego prowadzono dalsze intensywne badania dotyczące zastosowania metod instrumentalnych do oznaczania związków siarki pełniących rolę induktorów reakcji jodo-azydkowej. Profesorowie Witold Ciesielski i Zbigniew Kudzin opisali oznaczenia związków tiofosforowych indukujących reakcję jodo-azydkową prowadzone metodami miareczkowymi, spektrofotometrycznymi i kulometrycznymi oraz detekcję tych związków w chromatografii cienkowarstwowej.
W. Ciesielski i R. Zakrzewski wykorzystywali reakcję jodo-azydkową do detekcji tioli, aminokwasów, amin biogennych, dipeptydów i amfetamin w TLC oraz do ilościowego oznaczania tioli metodą chromatografii cienkowarstwowej wykorzystując technikę analizy obrazu (image analysis). Derywatyzacja za pomocą fenyloizotiocyjanianu umożliwiła detekcję związków z grupą aminową. Uzyskanie przez prof. W. Ciesielskiego grantu aparaturowego umożliwiło zakup chromatografu cieczowego i rozpoczęcie oznaczeń tioli metodą HPLC, co doprowadziło do opracowania czułych metod oznaczania biologicznie czynnych tioli w materiale biologicznym. W 2010r. dr Robert Zakrzewski obronił pracę habilitacyjną pt. „Reakcja jodo-azydkowa w chromatografii cieczowej”. Obecnie poszukuje on nowych chromatograficznych metod (HPLC, TLC) oznaczania związków biologicznie czynnych i ich metabolitów w płynach ustrojowych (mocz, osocze, erytrocyty).
W. Ciesielski i Z. Kudzin zaproponowali wykorzystanie układu: bezwodnik kwasu trifluorooctowego-jodek sodu do miareczkowych i spektrofotometrycznych oznaczeń sulfotlenków, nitronów i rodników nitroksylowych oraz do detekcji tych związków w chromatografii cienkowarstwowej.
W. Ciesielski z zespołem pracowników i doktorantów Zakładu Analizy Instrumentalnej opracował kulometryczne i objętościowe metody miareczkowania tioli jodem w środowisku zasadowyma także opisał kulometryczne miareczkowania tioli, disulfidów i pestycydów tiofosforowych anodowo wytwarzanym chlorem. Metody te zastosowano do oznaczania biologicznie czynnych tioli w preparatach farmaceutycznych.
Grant aparaturowy KBN umożliwił zakup skomputeryzowanej aparatury do prowadzenia oznaczeń woltamperometrycznych i rozpoczęcie przez W. Ciesielskiego i S. Skrzypek woltamperometrycznych oznaczeń tioli. Podobną tematyką w tamtym czasie zajmował się prof. F. Banica z Norwegian University of Science and Technology, Trondheim, Norwegia. Po nawiązaniu współpracy z prof. F. Banica w 2005 r. badano selenometioninę jako katalizator redukcji jonów niklu na elektrodzie rtęciowej, a także wybrane aminokwasy pełniące tę samą funkcję. Przy współpracy z prof. Valentinem Mirčeskim (Sv. Kiril i Metodij University, – Skopje, Macedonia ) badano mechanizmy zachodzących reakcji elektrodowych biologicznie czynnych związków z grupą guanidynową.
Dr S. Skrzypek w 2009r. została koordynatorem sieci "Education of Modern Analytical and Bioanalytical Methods" międzynarodowego programu CEEPUS (Central European Exchange Program for University Studies) w Uniwersytecie Łódzkim. Dr Sylwia Smarzewska jest koordynatorem uniwersyteckim kolejnej sieci CEEPUS o nazwie "Food Safety for Healthy Living". Udział w sieciach CEEPUS umożliwia pracownikom, doktorantom i studentom wyjazdy na staże zagraniczne.
W 2012r. dr Sławomira Skrzypek obroniła rozprawę habilitacyjną pt. ”Związki z grupą guanidynową jako elektrokatalizatory redukcji wodoru: mechanizm elektrodowy i woltamperometryczne oznaczanie” i uzyskała etat prof. nadzwyczajnego.
W. Ciesielski z zespołem pracowników i doktorantów opracował czułe woltamperometryczne metody oznaczeń wielu organicznych związków biologicznie czynnych z wykorzystaniem kroplowej elektrody rtęciowej, elektrody z amalgamatu srebra oraz niemodyfikowanych i modyfikowanych elektrod węglowych. Metody te stosowano do oznaczeń pestycydów i leków w próbkach naturalnych. Metody woltamperometryczne i spektrofotometryczne były także wykorzystywane do badania interakcji DNA.
W Zakładzie Analizy Instrumentalnej prowadzone były również prace dotyczące spektrofotometrycznego oznaczanie związków siarki z wykorzystaniem N,N-dimetylo-p-fenylenodiaminy oraz wykorzystania techniki image analysis w chromatografii cienkowarstwowej do ilościowego oznaczania fosfolipidów, siarczków, pestycydów i aminokwasów.
Dr Dariusz Guziejewski w Zakładzie Analizy Instrumentalnej realizuje kilka tematów z zakresu elektrochemii obejmujących: 1) elektroanalizę chemiczną wybranych substancji biologicznie czynnych z wykorzystaniem nowych metod woltamperometrycznych takich jak woltamperometria z falą prostokątną, woltamperometria różnicowa fali prostokątnej czy warianty analizy z użyciem techniki SWV. 2) prowadzi modelowanie wybranych procesów elektrodowych w technice SWV i pokrewnych, co ma na celu lepsze zrozumienie mechanizmów reakcji elektrodowych oraz optymalizację warunków pomiarowych dla uzyskania jak największej czułości i precyzji pomiarów; 3) w badaniu kinetyki reakcji elektrodowych skupia się na badaniu szybkości reakcji elektrodowych, a w ramach wykazywanego osiągnięcia naukowego w postępowaniu habilitacyjnym przedstawił charakter i użyteczność wpływu amplitudy fali prostokątnej w technice SWV i jej pokrewnych. Pozwala mu to na szacowanie kinetyki bez potrzeby zmiany ram czasowych eksperymentu. W ramach tej tematyki zostały zrealizowane dwa projekty sfinansowane przez Narodowe Centrum Nauki, które umożliwiły unowocześnienie aparatury naukowej Zakładu i przyczyniły się do rozszerzenia tematyki prowadzonych badań; 4) ponadto prowadzi badania nowych materiałów elektrokatalitycznych: które mogą być wykorzystane do zwiększenia efektywności i selektywności różnych reakcji elektrodowych, takich jak oznaczanie nadtlenku wodoru, ale również utlenianie metanolu, redukcja dwutlenku węgla czy rozszczepianie wody. W tym temacie zgłoszono rozwiązanie patentowe dotyczące solwotermalnej metody syntezy selenku niklowo-kadmowego; 5) dr Guziejewski rozwija również i charakteryzuje nowe elektrochemiczne techniki pomiarowe, zajmuje się m.in. projektowaniem i opracowywaniem nowych protokołów pomiarowych oraz oceną ich skuteczności i stosowalności. Celem jest stworzenie zaawansowanych narzędzi i technik umożliwiających szczegółowe badanie procesów elektrodowych oraz ich zastosowanie w praktyce. W wyniku tych prac powstały 3 zgłoszenia patentowe.
W 2024 r. dr D. Guziejewski uzyskał stopień doktora habilitowanego na podstawie pracy habilitacyjnej pt. „Amplituda fali prostokątnej jako wielowymiarowe narzędzie diagnostyczne w pomiarach elektrochemicznych”.
Wprowadzone przez dr Sylwię Smarzewską w Zakładzie Analizy Instrumentalnej elektrochemiczne badania grafenu i jego pochodnych obejmują analizę właściwości różnych typów elektrod pracujących (dyskowych, pastowych, drukowanych) wytworzonych z zastosowaniem modyfikacji lub bazy z grafenu i jego pochodnych (tlenku grafenu i zredukowanego tlenku grafenu). Analizie poddaje się zarówno właściwości strukturalne jak i elektro- i fizykochemiczne wytworzonych elektrod. Przyczynia się to do zastosowań ww. elektrod w oznaczeniach elektrochemicznych kolejnych substancji elektroaktywnych (leków, pestycydów, metali).
W 2024 r. dr S. Smarzewska uzyskała stopień doktora habilitowanego na podstawie pracy habilitacyjnej pt. „ Zastosowanie materiałów grafenopochodnych do celowanej funkcjonalizacji elektrod pracujących, ich aktywacja i aplikacja do wysokoczułych oznaczeń w matrycach prostych i złożonych”.
Badania nad pochodnymi grafenu oraz ich możliwym zastosowaniem do rozróżniania różnych typów DNA (grant IDUB „Multidyscyplinarne badanie interakcji DNA – Kierownik dr hab. Sylwia Smarzewska) przyczyniły się do wynalezienia pięciu nowych typów elektrod (5 zgłoszeń do Urzędu Patentowego RP, dwa zgłoszenia europejskie w trybie EPO oraz jedno zgłoszenie patentowe międzynarodowe w trybie PCT). Prawa do produkcji i sprzedaży dwóch z ww. elektrod, w ramach licencji, nabyła od UŁ szwedzka firma RedoxMe.
Pozostałe zgłoszenia patentowe zespołu dr hab. Sylwii Smarzewskiej dotyczyły głównie szeroko pojętej analizy spożywczej. Dwa z tych zgłoszeń powstały przy współudziale spółki z branży spożywczej, a jedno znalazło nabywcę, co poskutkowało zawarciem umowy prawa pierwokupu patentu.
Elektroanaliza próbek spożywczych była także przedmiotem projektu realizowanego ze spółką Miramar, w ramach inicjatywy trójstronnej ScienceHub. W ramach projektu opracowano warunki produkcji oleju z prażonego sezamu. Olej, sygnowany logiem Wydziału Chemii UŁ trafił na rynek w grudniu 2023 r.
W latach 2022-2024 w Zakładzie Analizy Instrumentalnej realizowany był grant NCN-u pt. „Elektrochemiczne sensory gazowe do detekcji nadtlenku wodoru” kierowany przez prof. Valentina Mirčeskiego.
Opisane powyżej tematy badań w Zakładzie Analizy Instrumentalnej były realizowane w ramach 13 prac doktorskich oraz 5 rozpraw habilitacyjnych.
Od 1 stycznia 2007 r. Zakład Analizy Instrumentalnej został przekształcony w Katedrę Analizy Instrumentalnej a 1 października 2009 r. w wyniku połączenia Katedry Chemii Ogólnej i Nieorganicznej oraz Katedry Analizy Instrumentalnej została utworzona Katedra Chemii Nieorganicznej i Analitycznej, w strukturze której znalazł się Zakład Analizy Instrumentalnej kierowany przez prof. Witolda Ciesielskiego. W roku 2013 dr hab. prof. UŁ Sławomira Skrzypek została kierownikiem nowego Zakładu Elektroanalizy i Elektrochemii, a rok później kierownikiem Katedry Chemii Nieorganicznej i Analitycznej.
W Zakładzie Elektroanalizy i Elektrochemii prowadzone są badania z obszaru elektroanalizy wykorzystujące zaawansowane materiały elektrodowe.Początkowo badania w Zakładzie koncentrowały się na wykorzystaniu elektrody srebrnej z odnawialnym filmem amalgamatu srebra do opracowania procedur woltamperometrycznego oznaczania głównie pestycydów, ale także antybiotyków jonoforowych i leków weterynaryjnych. Z czasem do badań zaczęto stosować niemodyfikowane elektrody stałe na bazie węgla (z węgla szklistego, grafitu pirolitycznego z prostopadle ułożonymi warstwami grafitowymi, z diamentu domieszkowanego borem). W przypadku elektrod diamentowych domieszkowanych borem dodatkowym, istotnym aspektem było zbadanie wpływu obróbki wstępnej powierzchni tych elektrod (terminacji powierzchni) oraz poziomu domieszkowania diamentu borem na ich właściwości i parametry analityczne. Kolejnym kierunkiem badań było wytworzenie niemodyfikowanych planarnych i porowatych elektrod diamentowych domieszkowanych borem z wykorzystaniem zarówno konwencjonalnej metody chemicznego osadzania z fazy gazowej wspomaganego plazmą mikrofalową (MW-PECVD), jak i metody MW-PECVD z dodatkowym systemem „linear-antena”. Wytworzone elektrody zostały poddane kompleksowej charakterystyce oraz wykorzystane do badania i oznaczania neuroprzekaźnika (dopamina).
W Zakładzie prowadzone były również badania nad otrzymaniem, charakterystyką i zastosowaniem modyfikowanych powierzchniowo elektrod węglowych za pomocą różnych materiałów węglowych (wielościenne i jednościenne nanorurki węglowe, zredukowany tlenek grafenu, nanorogi węglowe). Elektrody te zastosowano do elektroanalizy kolejnych związków biologicznie czynnych. Ciekawym obszarem badań było otrzymanie materiałów kompozytowych do modyfikacji elektrod metalicznych (platyna, złoto) i węglowych (węgiel szklisty) na bazie polimeru przewodzącego (poli(3,4-etyleno-1,4-dioksytiofenu, PEDOT) w połączeniu z nanomateriałami (nanocząstki złota) i innymi substancjami (np. chitozan). Otrzymane materiały były badane pod kątem ich zastosowania do budowy elektrochemicznych sensorów enzymatycznych z unieruchomioną oksydazą glukozową oraz unieruchomioną laktazą, które umożliwiały oznaczenie glukozy i polifenoli w różnych środowiskach, w tym w produktach naturalnych.
Kolejnym kierunkiem badań było wytworzenie i charakterystyka modyfikowanych objętościowo pastowych elektrod węglowych oraz ceramicznych elektrod węglowych przygotowywanych z wykorzystaniem metody zol-żel. Badania pastowych elektrod węglowych modyfikowanych objętościowo zredukowanym tlenkiem grafenu otrzymanym metodami chemicznymi i termicznymi były prowadzone w ramach projektu Preludium finansowanego przez Narodowe Centrum Nauki, którego kierownikiem była dr Mariola Brycht. Warto nadmienić, że dr Brycht odbyła roczny staż na Charles University w Pradze, ośrodku mającym znaczne osiągnięcia w obszarze wytwarzania elektrod diamentowych domieszkowanych borem. Opisane powyżej tematy badań były realizowane w ramach 6 prac doktorskich, a także 1 rozprawy habilitacyjnej (dr hab. Marioli Brycht).
Zakład współpracuje z partnerami z uczelni zagranicznych: University of Graz (Austria), Charles University (Praga, Czechy), Pardubice University (Czechy), Ankara University (Turcja), EG University (Izmir, Turcja), Canakkale University (Canakkale, Turcja). W ramach wspólnych projektów badawczych NAWA podjęto współpracę z Uniwersytetem w Bratysławie, której tematem są perspektywiczne czujniki elektrochemiczne oparte na nietradycyjnych, węglowych materiałach elektrodowych jako narzędzia analityczne przydatne w analizie farmaceutycznej, klinicznej, spożywczej i środowiskowej.
W 2024 r. stopień doktora habilitowanego uzyskała dr Mariola Brycht na podstawie pracy habilitacyjnej pt. „Materiały elektrodowe na bazie wybranych odmian alotropowych węgla do zastosowań w elektroanalizie”.
Zmiana struktury UŁ w 2024 r. spowodowała zakończenie funkcjonowania zakładów (Zakładu Analizy Instrumentalnej i Zakładu Elektroanalizy i Elektrochemii) i powołanie zespołów naukowych w Katedrach.
W Katedrze Chemii Nieorganicznej i Analitycznej w Pracowni Zagrożeń Środowiska prowadzone są badania zawartości toksyn sinicowych w wodzie i materiale biologicznym; opracowania nowych metod analitycznych technikami GC, HPLC i EC substancji farmakologicznie czynnych oraz ksenobiotyków z materiału biologicznego i prób środowiskowych (woda, powietrze, gleba), a także oznaczania substancji kontaminujących oraz opracowanie metod analizy surowców, półproduktów i produktów dla celów analizy przemysłowej i technicznej. Pracownia wyposażona jest w chromatograf cieczowy (z detektorami DAD i FLD), chromatograf gazowy z detekcją FID, ECD oraz MS/MS i aparat do elektroforezy kapilarnej. W dniu 15 lutego 2010 roku Uniwersytet Łódzki podpisał umowę z Urzędem Marszałkowskim w Łodzi o dofinansowanie projektu pn. Zwiększenie bezpieczeństwa mieszkańców narażonych na zagrożenia naturalne w zbiornikach retencyjnych województwa łódzkiego przez modernizację sprzętu i wprowadzenie innowacyjnych metod monitoringu w Pracowni Zagrożeń Środowiska Uniwersytetu Łódzkiego w ramach Regionalnego Programu Operacyjnego Województwa Łódzkiego na lata 2007-2013.

Zatrudniony w Katedrze Chemii Nieorganicznej i Analitycznej w 2019 r. dr Łukasz Półtorak wprowadził nową tematykę naukową polegającą na badaniach spolaryzowanych granic fazowych dwóch niemieszających się ze sobą cieczy z wykorzystaniem metod elektrochemicznych, mikroskopowych i spektroskopowych. W 2021 r. przedstawił zatwierdzoną przez Radę Wydziału Chemii pracę habilitacyjną pt. „Elektrochemiczne badania wybranych związków z grupą aminową na niemodyfikowanych oraz modyfikowanych spolaryzowanych granicach fazowych typu ciecz-ciecz”. Od roku 2022 już jako doktor habilitowany pracuje na stanowisku profesora uczelni. Jest liderem grupy badawczej „Electrochemistry@Soft Interfaces”, w którym realizowanych jest wiele grantów naukowych finansowanych przez Narodowe Centrum Nauki, Narodową Agencję Wymiany Akademickiej, (z ang.) Royal Society of Chemistry oraz Komisję Europejską. Zainteresowania naukowe dr. hab. Łukasza Półtoraka bazują na jego wcześniejszych doświadczeniach, które zdobył na Uniwersytecie w Bielefeld (Niemcy) jeszcze jako magistrant, Uniwersytecie Lotaryńskim (Francja) jako doktorant prowadzący badania pod opieką dr. hab. Alain Walcarius oraz Uniwersytecie Technicznym w Delft (Holandia) gdzie na stażu podoktorskim współpracował z prof. Ernst Sudhölter. Na Wydziale Chemii Uniwersytetu Łódzkiego, jako lider międzynarodowego zespołu, nadzoruje prace badawcze związane z (i) badaniem związków psychotropowych (np. kokaina, heroina, amfetamina, metamfetamina itp.) z wykorzystaniem granic fazowych typu ciecz-ciecz, (ii) tworzeniem nowych układów elektroanalitycznych opartych o miniaturyzację (wytwarzanie porowatych membran, kapilar, nano- i mikroelektrod), (iii) wykorzystaniem technik druku 3D do zastosowań elektrochemicznych i elektroanalitycznych, (iv) wytwarzaniem nowych materiałów drukowalnych (opartych na żelach, materiałach termoplastycznych oraz lepkich cieczach), (v) prowadzeniem reakcji wspomaganych elektrochemicznie, (vi) badaniem zjawisk związanych z elektrochemicznie kontrolowanymi przejściami jonowymi oraz (vii) analizowaniem biomimetycznych granic fazowych (np. układy oparte na lipidach). W ramach prowadzonych prac badawczych, dr hab. Łukasz Półtorak współpracuje z naukowcami z wielu renomowanych jednostek naukowych. Przykłady obejmują Instytut Chemii Fizycznej J. Heyrovsky w Pradze (Czechy), Uniwersytet Palackiego w Ołomuńcu (Czechy), Netherlands Forensic Institute w Hadze (Holandia), Uniwersytet Lotaryński w Nancy (Francja), czy też Henan University w Kaifeng (Chiny).

Prace z zakresu chemii analitycznej, które dotyczyły wykorzystania nowych odczynników do wykrywania i oznaczania związków siarki były zainicjowane i prowadzone przez prof. Mieczysława Wrońskiego w Katedrze Technologii Chemicznej i Ochrony Środowiska, od końca lat 50. do roku 1997. Przedmiotem badań były m. in. dwutiofluoresceina, rtęciowana fluoresceina i kwas o-hydroksyrtęciobenzoesowy. W konsekwencji Profesor Wroński znany jest w literaturze chemicznej jako twórca tiomerkurymetrii – działu analizy chemicznej, u podstaw której leży tworzenie stabilnego wiązania pomiędzy atomami siarki i rtęci. Procedury analityczne opracowane w ramach tego obszaru znalazły zastosowanie w badaniach środowiskowych oraz w badaniach nad przebiegiem procesów technologicznych.
Prof. Edward Bald, uczeń prof. Wrońskiego, od początku lat 80. prowadził badania nad nowymi odczynnikami derywatyzującymi związki tiolowe w ich analizie z wykorzystaniem technik wysokosprawnej chromatografii cieczowej (HPLC) i kapilarnej elektroforezy (CE).
W połowie lat 90. prof. Edward Bald stworzył Zakład, przekształcony w 2010 r. w Katedrę Chemii Środowiska (KChŚ). Środki finansowe uzyskane dzięki jego staraniom w postaci kilku grantów badawczych i inwestycyjnych, umożliwiły wyposażenie laboratoriów w nowoczesną, jak na owe czasy, aparaturę badawczą, m.in. chromatografy cieczowe, aparat do elektroforezy kapilarnej oraz automatyczne procesory próbek biologicznych. Prowadzone pod jego kierunkiem badania nakierowane były w głównej mierze na opracowywanie nowych metod analitycznych i ich aplikację do próbek środowiskowych, w tym próbek biologicznych takich jak krew i mocz. Wieloletnie badania, obejmujące tzw. zdrowie środowiskowe, prowadzone we współpracy z licznymi ośrodkami medycznymi z kraju i zagranicy, skierowały zainteresowania naukowe Zespołu w stronę aplikacji biomedycznych. Odzwierciedleniem tego faktu była tematyka prowadzonych w Katedrze prac doktorskich. Obejmowała ona m.in. badania dotyczące wyznaczania statusu red-ox tioli w płynach ustrojowych człowiekaoraz określenie mechanizmów aterogennego działania homocysteiny i jej metabolitów na organizm ssaków.
Zdobyte we wcześniejszych latach doświadczenie prof. E. Balda z zakresu syntezy organicznej umożliwiło prowadzenie równoległego kierunku badań, który skupiał się na syntezie nowych, selektywnych w stosunku do związków tiolowych, odczynników derywatyzujących. W zakresie technik elektromigracyjnych badania Zespołu dotyczyły głównie opracowywania nowych metod oznaczania wybranych egzo- i endogennych związków tiolowych w produktach spożywczych i preparatach farmaceutycznych.
W roku 2011 kierownictwo Katedry Chemii Środowiska objął prof. dr hab. Rafał Głowacki, który w tym samym roku obronił pracę habilitacyjną pt. „Badanie mechanizmu homocysteinylacji białek z wykorzystaniem wysokosprawnej chromatografii cieczowej”. Trzy lata później pracę habilitacyjną zatytułowaną „Analiza próbek biologicznych na zawartość metabolicznie spokrewnionych związków siarki” przedstawiła dr Grażyna Chwatko. W roku 2018 stopień dra hab. uzyskał inny członek zespołu, dr Paweł Kubalczyk, po przedstawieniu rozprawy pt. „Elektroforeza kapilarna próbek biologicznych z wykorzystaniem metod zatężania analitów on-line”.
W 2024 r. stopień doktora habilitowanego uzyskała dr Kamila Borowczyk na podstawie rozprawy pt. „Upraszczanie procedur analitycznych dedykowanych chromatograficznemu oznaczaniu wybranych, biologicznie ważnych związków siarki”.
Obecne zainteresowania naukowe prof. Rafała Głowackiego dotyczą wykorzystania technik separacyjnych w fazie ciekłej (HPLC, CE) oraz gazowej (GC) w analityce próbek o złożonych matrycach, w tym badania oddziaływań aminokwasów tiolowych z białkami, śledzenia procesów potranslacyjnej modyfikacji białek tiolaktonem homocysteiny oraz poszukiwania nowych metabolitów. Obszar badawczy eksplorowany przez Panią dr hab. Grażynę Chwatko, prof. UŁ dotyczy w dużej mierze chromatograficznej analizy próbek biologicznych, w tym tkanek roślinnych i zwierzęcych. Badania z zakresu możliwości zatężania analitów w trybie „on-line” w CE znajdują się z kolei w kręgu zainteresowań dra hab. Pawła Kubalczyka, prof. UŁ. We wszystkich przypadkach nieodzownym elementem prowadzonych eksperymentów jest rozwijanie nowych, oryginalnych procedur przygotowania próbek, które w zdecydowanej większości bazują na technikach ekstrakcji ciecz-ciecz oraz ciecz-ciało stałe. Dzięki staraniom prof. Głowackiego, w ostatnich latach znacznie poszerzona została baza aparaturowa Katedry. Zakupionych zostało kilka chromatografów, w tym m.in. chromatograf cieczowy sprzężony z detektorem mas (HPLC-MS/MS) oraz chromatograf gazowy wyposażony w podobny sposób detekcji (GC-MS). W istotnym zakresie poszerzone zostało również zaplecze lokalowe. Działania te umożliwiły zintensyfikowanie prac badawczych prowadzonych przez dr Justynę Piechocką, która w nieodległej przyszłości będzie ubiegała się o uzyskanie stopnia doktora habilitowanego. Opracowywane w KChŚ nowoczesne metody, które bazują głównie na nowoczesnych technikach separacyjnych, budzą duże zainteresowanie społeczności naukowej, czego odzwierciedleniem jest znaczna liczba cytowań prac opublikowanych przez członków Zespołu. Z praktycznego punktu widzenia nie mniej istotna jest współpraca pracowników KChŚ z szeroko pojętym otoczeniem gospodarczym. W kontekście finansowania badań naukowych należy natomiast wspomnieć o środkach pozyskanych przez pracowników, zarówno ze źródeł zewnętrznych (6 grantów NCN) jak i w ramach konkursów wewnątrzuniwersyteckich. Pozwoliło to na uzupełnienie bazy aparaturowej o kolejne specjalistyczne przyrządy, w tym. chromatografy cieczowe, spektrofotometr UV-Vis oraz aparaturę niezbędną na etapie przygotowania próbek do analizy.
Pracownicy KChŚ byli inicjatorami i twórcami programu studiów podyplomowych zatytułowanych „Chromatografia i techniki pokrewne we współczesnej analizie”, które uruchomiono w roku 2016, i które funkcjonowały na Wydziale Chemii UŁ przez kolejne cztery lata pod kierownictwem dr hab. Grażyny Chwatko, prof. UŁ.
Od szeregu lat pracownicy Katedry prowadzą owocną współpracę naukową z ośrodkami w kraju i za granicą. W obszarze roli tiolaktonu homocysteiny w rozwoju chorób układu sercowo-naczyniowego współpraca obejmuje m.in. wspólne badania z prof. dr. hab. Hieronimem Jakubowskim z Rutgers the State University of New Jersey. W latach wcześniejszych miała natomiast miejsce współpraca z prof. I. M. R. Wright z University of Newcastle, która dotyczyła wpływu siarkowodoru na układ krwionośny noworodków. Specyfika wykorzystywanych technik analitycznych powoduje, że wiele wspólnych projektów badawczych pracownicy Katedry prowadzą obecnie z naukowcami z Wydziału Biologii i Ochrony Środowiska Uniwersytetu Łódzkiego.
Starania prof. Witolda Ciesielskiego, członka Komitetu Chemii Analitycznej PAN i Komisji Nauczania Chemii Analitycznej, doprowadziły w 2010 r. do utworzenia nowej specjalności na Wydziale Chemii – analityki chemicznej, która od października 2012r. została przekształcona w kierunek studiów.
Katedry Chemii Nieorganicznej i Analitycznej oraz Ochrony Środowiska prowadzą współpracę naukową z następującymi ośrodkami zagranicznymi: Rutgers the State University of New Jersey (USA), University of Newcastle (Australia), Catholic University of Leuven (Belgia), Norwegian University of Science and Technology (Trondheim, Norwegia), Sv. Kiril i Metodij University (Skopje, Macedonia), Canakkale Onsekiz Mart University (Canakkale, Turcja), University of Novi Sad (Nowy Sad, Serbia), Karl Franzens University (Graz, Austria), Universitat de Valencia (Valencia, Hiszpania). Współpraca ta umożliwia wyjazdy pracowników, doktorantów i studentów na staże zagraniczne i owocuje wspólnymi publikacjami.
